孙燕院士解读2018年ASCO临床肿瘤学进展
目前医学发展很快,不要再把肿瘤疾病当成致命性疾病,而是要作为慢性疾病来看待,希望国家能大力支持转化研究,早日把这些疗法用于小动物临床上来。我们兽医人都加油。
为了评价年度临床肿瘤学重大进展,近年来ASCO在年末都组织专家讨论并在美国《临床肿瘤学杂志》(J Clin Oncol)上发表供广大同行参考。我们也每年在年初加以介绍并写出评述。但是,大家翘首以待ASCO的文章最近才发布。在此以前我们看到的是CA杂志(CA Cancer J Clin)发表的美国《2018癌症数据报告》,《J Thorac Oncol》杂志发表的国际肺癌研究学会(IASLC)盘点2017年胸部恶性肿瘤进展和《J Clin Oncol》杂志发表的免疫治疗进展,可能让大家看得眼花缭乱。其实,仔细读来最重要的是以下四点,在这里写出与大家分享。
一、美国癌症发病率死亡率持续下降
CA杂志这篇《2018癌症数据报告》无疑是我们最关心的内容,结果与往年相差不大。2018年美国将有170余万例发病;61万人死于癌症。男性发病率每年以2%的速度稳定下降;而女性则变化不大,其中女性乳腺癌、子宫癌、甲状腺癌和黑色素瘤发病率还有升高。尽管如此,美国癌症总体死亡率与1991年相比下降了26%,他们将这归功于控烟、技术的发展带来的早期诊疗进步。男性一生中患癌的概率是39.7%,女性是37.6%。肺癌、前列腺癌、乳腺癌和结直肠癌仍然是四大杀手。他们的口号是:推动全民抗癌斗争,广泛应用现有的抗癌知识包括控烟、增加宫颈和大肠癌的筛查,加强HPV疫苗接种,对弱势人群加以扶持。
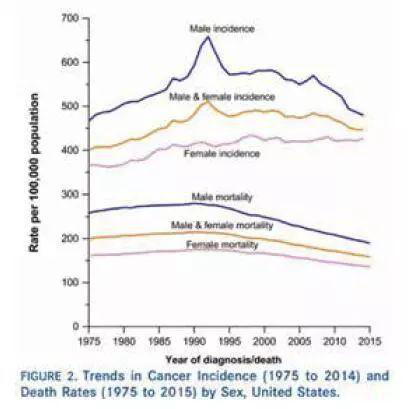
我们国家癌症中心最近发表了“加强癌症检测,助力癌症防控”的文章,其中报道了我国癌症的发病趋势和2000~2013死亡率趋于平稳的情况,并且指出防控的重点是控烟、饮食和感染[中华肿瘤杂志 2018; 40(1):1-4.]。美国的经验无疑值得我们借鉴。
二、免疫治疗发展迅猛
+
通过调动机体自身的抗病能力与基本斗争是临床医学的永恒课题。我们的祖先早在2000多年前就重视扶正祛邪。而很多传染性疾病通过免疫治疗达到根治甚至绝迹,这无疑是临床医学最精彩的篇章。
对于癌症,如何通过调动患者的免疫功能加以控制,也有半个多世纪的探索,但由于肿瘤病因复杂,而以前的免疫治疗大多是非特异性免疫增强,所以一直进展不大。
PNAS杂志(Proc Natl Acad Sci USA)最近发布200万例癌症患者的总结,总体来说癌症发病率随年龄的增长而提高,根本原因是由于DNA缺损的积累,导致细胞免疫功能的衰老。近年来,主要进展是认识到肿瘤细胞表达PD-L1和特异性过继免疫CAR-T的发展。
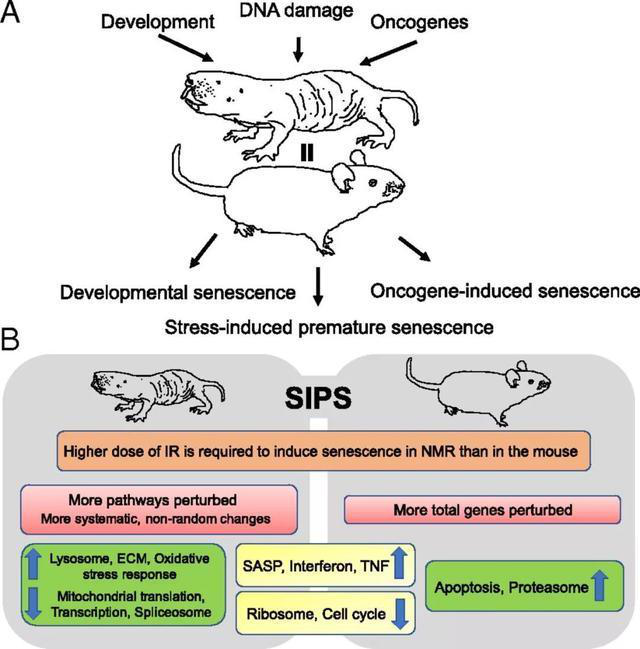
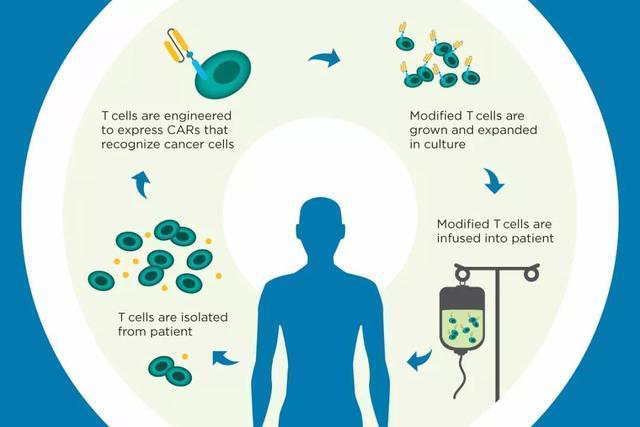
1. CAR-T细胞免疫疗法
ASCO的评述将CAR-T细胞免疫疗法列为2017年最重要的临床进展。CAR-T,全称是 chimeric antigenreceptor T-cell immunotherapy(嵌合抗原受体T细胞免疫疗法)。对CAR-T疗法已经有几十年的研究,通过训练患者自身的免疫细胞,利用患者自身的免疫细胞来清除癌细胞治疗癌症,是一种细胞疗法,而不是一种药。制备的步骤是:(1)从癌症患者身上分离免疫T细胞。(2)利用基因工程技术给T细胞加入一个能识别肿瘤并且同时激活T细胞杀死肿瘤细胞的嵌合抗体,使普通T细胞变成具有强大作用的CAR-T细胞。它不再是一个普通的T细胞,它是一个带着GPS导航,随时准备找到癌细胞,并且发动自杀性袭击,与之同归于尽的“恐怖分子”T细胞。(3)体外培养,大量扩增CAR-T细胞,一般一个患者需要几十亿,乃至上百亿个CAR-T细胞,往往患者体形越大,需要的细胞越多。(4)把扩增好的CAR-T细胞输回患者体内。
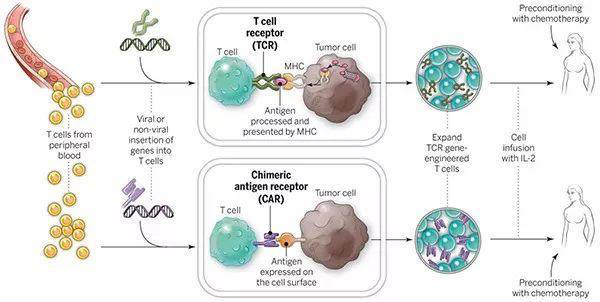
从2016年11月到2017年10月这一年间,美国FDA共批准了两个过继免疫疗法(adoptive immune therapy)。2017年8月,FDA批准了第一个CAR-T细胞疗法Tidagenlecleucel(商品名:Kymriah)用于治疗复发的青少年急性淋巴细胞白血病,结果80%的患者获得完全缓解,有的已经生存超过10年。
2017年10月,第二个CAR-T细胞疗法Axicabtagene ciloleucel(商品名:Yescarta),用于治疗B细胞淋巴瘤,也已经上市。
2. PD-L1/PD-1免疫检查点抑制剂
PD-L1/PD-1抑制剂已经有了比较广泛的研究。FDA已经批准其中4种进入临床。2017年Pembrolizumab(商品名:Kaytruda)成为第一个获批准的广谱免疫制剂。不论肿瘤在何部位,只需有特定基因变异——高微卫星不稳定性或错配修复缺陷(MSI-H或dMMR)这两项特征,就可以应用。这在很大程度上类似中医的“异病同治”。
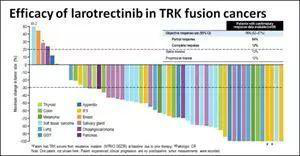
另一个很有希望的新药物,Larotrectinib,针对一个罕见的肿瘤基因变异(TRK基因融合),也可以用于各种肿瘤类型。这个药物现在进行Ⅰ/Ⅱ期临床试验,如果通过FDA批准,就有望成为第一个“与肿瘤无关”的广谱靶向疗法。
三、靶向药物发展迅速且趋向成熟
+
2017年,美国FDA批准了13种新的靶向治疗,用于白血病、多发性骨髓瘤、卵巢癌、乳腺癌、肺癌。截至2017年,美国NCI的数据库中靶向药物已经涵盖了27种肿瘤。其中最多的是肺癌和淋巴瘤都是16种,其次是白血病15种、乳腺癌13种、肾癌11种、皮肤癌12种、黑色素瘤9种,其他分别为头颈部癌8种、多发性骨髓瘤7种、妇科肿瘤5种、大肠癌6种、消化系统癌5种、胰腺癌3种、胃癌2种、甲状腺癌4种、膀胱癌5种、肉瘤3种。说明在临床上超过半数患者在一定时期应考虑是否可以采用靶向药物。
NSCLC的靶向治疗第一代EGFR-TKI研究最多,临床应用的适应证也已经比较明确,有EGFR基因突变的患者无论早期或晚期都可以从中获益;耐药患者有T790M突变的患者接受第二代TKI奥希替尼(Osimertinib,AZD9291)治疗疗效明显,而且认识到具有ALK-EML4融合基因的患者也可能从PD-L1/PD-1抑制剂治疗中获益;第三代的TKI Olmutinib(奥姆替尼)疗效也比较肯定。具有ALK-EML4融合基因的患者应用克唑替尼的疗效突出,第二代的药物也进入临床试验。在临床上应用已经比较成熟,有效率可达60%~80%,而且不良反应少,在一定程度上在敏感患者可以取代化疗。

另外,特别令人鼓舞的是抗PD-L1/PD-1单抗与化疗联合应用。2017年5月Pembrolizumab(派姆单抗)联合化疗治疗非鳞NSCLC的结果,联合组有效率56.7%,而化疗组为31.7%;PFS分别是19.0个月和8.9个月。2017年12月,罗氏Atezolizumab+贝伐珠单抗+化疗治疗之前未接受过化疗的晚期非鳞NSCLC患者,有效率分别为65%和48%;PFS分别为8.3个月和6.8个月。2018年1月16日,默沙东宣布一项入组614例患者的Ⅲ期临床研究Keynote189研究,PD-1单抗联合化疗有效率和生存率较单用化疗均有较大幅度的提高。
《新英格兰医学杂志》(N Engl J Med)2018年2月21日在线发布,拜耳公司针对17种肿瘤的抗癌新药Larotrectinib(LOXO-101)的最新研究数据。Larotrectinib是第一个口服、针对存在NTRK1、NTRK2或NTRK3基因融合的乳腺癌、胆管癌、结直肠癌、胃肠道间质瘤(GIST)、婴儿纤维肉瘤、肺癌、黑色素瘤、胰腺癌、阑尾癌、甲状腺癌等17种肿瘤的高选择性TRK抑制剂,可用于年龄4个月至76岁的儿童和成人病人,抗肿瘤客观有效率高达75%,而且安全性好。这无疑是新春过后肿瘤治疗进展最振奋人心的重磅好消息。
四、我国临床肿瘤学发展硕果累累
+
最近十余年,我国临床肿瘤学发展迅速,不但队伍不断扩大,而且水平已经有了很大的提升。如前所述,我国肿瘤登记已经覆盖近10%的人口,基本摸清了发病率和死亡率的趋势和主要致癌因素。
在治疗药物的研究上,尤其是靶向药物的研究已经追赶欧美国家,在亚洲领先。
十五期间,我们上市的有重组人血管内皮抑素(恩度),2018年1月2日于《Oncol Ther》杂志上在线发表的长篇综述《恩度在肿瘤治疗中的研究现状与进展》,介绍了恩度在肺癌、癌性胸腹水、黑色素瘤、骨及软组织肉瘤、胃癌、肾癌、乳腺癌、鼻咽癌、脑胶质瘤等肿瘤治疗结果,专著《重组血管内皮抑素》也于去年出版。
十一五期间上市的埃克替尼(凯美纳)在NSCLC治疗领域取得令世界瞩目的结果,不良反应低于其他两个第一代EGFR-TKI,已经完成与化疗联合持续给药可以进一步提高疗效、治疗晚期食管癌等研究。
十二五期间上市的阿法替尼和西达本胺在复发难治外周T细胞淋巴瘤中疗效突出。
十三五期间几个重大专项进展顺利,其中安罗替尼、普那布林和阿可拉定及两个PD-L1/PD-1抑制剂的研究结果将于今年的学术会议上发布。
目前,国内已有5家企业的CAR-T细胞治疗临床申请获得国家食品药品监督管理局受理并开始评审。中国在肿瘤靶向治疗及免疫治疗领域的新药研发、临床试验及政府新药审批加速都十分令人鼓舞。
除抗癌治疗技术进展外,以肿瘤病人为中心的诊断与治疗,还需要关注肿瘤病人的心理情感需求,改善生活质量,提供费效比更好的治疗,避免不必要的治疗,更好地辅助应用网络系统管理病人。

2018年ASCO临床肿瘤年度进展
美国2017年约170万新诊断肿瘤病例,超过1500万人相当于每20人就有1人是肿瘤生存者,曾患肿瘤或带瘤生存。肿瘤生存者数目在稳步攀升,预计到2040年这一数字将达到2600万,65岁以上人群中73%的人都将是肿瘤生存者。肿瘤死亡率在下降,肿瘤患者生存期在延长,2005年约有64%的诊断肿瘤患者生存10年以上,1975年时仅有35%。(J Clin Oncol. 2018年1月30日在线版. doi:10.1200/JCO.2017.77.0446)
2017年是肿瘤领域成果丰硕的一年,从2016年11月到2017年10月,美国FDA批准了31种新药用于治疗16种以上的肿瘤,最引人注目的是过继性细胞免疫疗法以及针对有特定基因异常的多种肿瘤的治疗。
第一种过继性细胞免疫疗法获批
2017年8月,FDA批准了第一种CAR-T疗法和第一种肿瘤基因疗法Tisagenlecleucel,几十年来人们训练机体免疫细胞杀伤肿瘤的努力终于有了回报。这一疗法的应用价值也是巨大的,Tisagenlecleucel是第一种真正治愈复发性儿童急性淋巴细胞白血病的疗法,ALL是最常见的儿童肿瘤之一。
2017年10月,FDA批准了第二种CAR-T疗法Axicabtagene ciloleucel,治疗特定类型成人淋巴瘤患者。还有其他CAR-T疗法在多发性骨髓瘤临床试验中显示不错的疗效。CAR-T疗法是有望改善肿瘤治疗的疗法,伴随而来的费用问题也需要引起注意。
肿瘤的“异病同治”
2017年肿瘤治疗领域另一项重大突破是首次根据肿瘤遗传学特征而不是发病部位治疗患者。Pembrolizumab (派姆单抗,Keytruda)于2017年获FDA批准治疗错配修复缺陷或高微卫星不稳定性(dMMR或MSI-H)的实体瘤患者。
另一种在研药物Larotrectinib 是靶向TRK融合蛋白的选择性抑制剂,许多不同类型肿瘤包括成人和儿童肿瘤都有TRK融合基因,Larotrectinib有望成为可治疗多种类型肿瘤的首个广谱靶向药物。
肺癌治疗进展
2017年非小细胞肺癌的一线治疗队伍再添两种新的治疗方法。
Alectinib(艾乐替尼,罗氏)一线治疗ALK突变肺癌患者。Pembrolizumab(派姆单抗,默沙东)单用或联合化疗用于NSCLC一线治疗。
Durvalumab(Imfinzi,阿斯利康)成为近年来首个证实在Ⅲ期局部晚期NSCLC有效的免疫治疗药物,被证实较目前标准治疗方案显著延缓疾病进展。
免疫检查点抑制剂已经改观了晚期非小细胞肺癌的治疗模式,目前已经有三种免疫检查点药物被批准,包括Nivolumab, Pembrolizumab和Atezolizumab。无基因突变的非小细胞肺癌患者中,如果PD-L1表达>50%,可考虑使用Pembrolizumab直接治疗;若PD-L1表达水平未知,且病理类型为非鳞,也可考虑使用Pembrolizumab联合化疗直接治疗。
在临床试验中,接受免疫检查点抑制剂治疗的患者较标准化疗患者,可生存更长。但免疫检查点抑制剂应用临床时间较短,长期生存效应还未知。ASCO报告预测,若所有NSCLC患者按适应证接受PD-1免疫检查点抑制剂治疗,每年可挽救25万例患者生命。
膀胱癌治疗进展
膀胱癌也是被免疫治疗改写治疗模式的瘤种。尿路上皮癌是晚期膀胱癌中最难治的一种,若仅接受标准化疗,只有5%的患者可以生存超过5年。近30年内,膀胱癌的治疗领域没什么进展。
随着免疫治疗的出现,膀胱癌的治疗发生了新的变化,免疫治疗为患者提供了一个相比标准化疗可生存更长、活得更好的机会。
Atezolizumab是第一个获FDA批准的膀胱癌免疫治疗药物,随后很快又有4种免疫治疗获批,包括Nivolumab, Avelumab, Pembrolizumab, Durvalumab。

脑胶质瘤进展
脑胶质瘤是最常见的成人脑部肿瘤之一,在目前的治疗技术下,只有不到10%的患者可生存5年。在2017年年度进展中,专家组也提到了两种新的可延长患者生存的治疗策略。
新技术TTF联合标准治疗可显著改善患者生存。TTF技术是一种肿瘤治疗电场,在标准的手术、放化疗后,携带TTF设备的患者生存时间可延长5个月,5年生存率大幅提升。TTF设备(Optune, Novocure Ltd)已于2015年被FDA批准。

将替莫唑胺添加至短疗程放疗,亦可显著改善患者生存(9.3个月vs. 7.6个月),且生活质量相似。携带MGMT基因甲基化的患者,在替莫唑胺联合放疗后,有更好的预后(13.5个月vs. 7.7个月)。
乳腺癌治疗进展
对于携带BRCA基因突变的乳腺癌患者,PARP抑制剂Olaparib(Lynparza, 阿斯利康)相比化疗,可延长患者生存。FDA已批准Olaparib用于BRCA基因突变的乳腺癌患者。
对于HER2阳性早期乳腺癌患者,帕妥珠单抗联合曲妥珠单抗双靶向治疗可降低浸润性乳腺癌发生风险,尤其是那些淋巴结阳性、HER2阳性、HR阴性患者发生浸润性乳腺癌风险。
在内分泌治疗方面,研究表明,对那些高风险乳腺癌患者延长内分泌治疗(10年vs. 5年)可降低乳腺癌复发风险及对侧乳腺癌风险。
前列腺癌治疗进展
报告指出,在具有里程碑意义的PROTECT研究10年随访 (N Engl JMed. 2016;375:1415-1424)显示,接受手术、放疗或主动监测的患者10年生存无显著差异,尽管主动监测可能带来更多的肿瘤恶化和转移风险。
另一项长期研究PIVOT研究显示,与主动监测相比,手术并未降低死亡风险,但手术患者在10年内发生更多的性功能障碍和尿失禁。
几种情况“少即是多”
化疗应考虑“少即是多”的情况:一项纳入了12800例患者的荟萃分析显示,接受3个月辅助化疗和6个月辅助化疗的患者预后相似,且副作用少。专家组表示,对于低风险的Ⅲ期结肠癌患者,3个月的短期疗程将可能成为新的治疗标准;对于高风险患者,短期持续治疗的决策须权衡复发风险及患者的耐受化疗能力和患者的偏好。

手术应考虑“少即是多”的情况:在黑色素瘤中,MSLT-I研究显示,清扫额外的淋巴结并不能延长生存。虽然可降低局部复发风险,但会导致更多的健康问题,尤其是淋巴水肿(N Engl J Med. 2017;376:2211-2222)。
在乳腺癌中,新的指南提出阴性切缘会降低乳房肿瘤切除术后二次手术的几率。一项大样本研究发现,2013~2015年间,接受一次乳房肿瘤切除术的比例稳定在67%,但接受二次手术比例降低了16%,即更少的女性接受了后续的乳房切除(JAMA Oncol. 2017;3:1352-1357)。该研究彰显了临床实践指南在降低过度治疗中的重要角色。
放疗应考虑“少即是多”的情况:在HPV相关的口咽癌患者治疗中,两项独立的临床试验发现,对有良好预后的患者,将标准放疗的剂量降低15%~20%,不影响生存期(J Clin Oncol. 2017;35:490-497; Lancet Oncol. 2017;18:803-811)。若在大样本临床试验中被证实,这些发现将改变低危HPV相关口咽癌(少吸烟史和小肿瘤)患者的标准临床治疗方案。
展望未来
报告指出了未来的研究方向:(1)靶向治疗,目前仍有很多已发现的靶点和通路,但尚无针对性的治疗,期待未来更多的新型药物研发成功。(2)精准医疗,期望未来精准医疗能在肿瘤预防中发挥更大的作用。(3)人群健康差异,基于地域、种族、经济状况等差异,癌症发病和治疗也存在差异,希望未来能更好了解人群差异,以提供合适的治疗方案。
